El átomo en la antigüedad
Los filósofos griegos discutieron mucho acerca de la naturaleza de la materia y concluyeron que el mundo era más simple de lo que parecía. Algunas de sus ideas de mayor relevancia fueron:


Demócrito y Leucipo
En el siglo V a. C., Leucipo sostenía que había un sólo tipo de materia y pensaba que si dividíamos la materia en partes cada vez más pequeñas, obtendríamos un trozo que no se podría cortar más. Demócrito llamó a estos trozos átomos ("sin división").
La filosofía atomista de Leucipo y Demócrito podía resumirse en:
1.- Los átomos son eternos, indivisibles, homogéneos e invisibles.
2.- Los átomos se diferencian en su forma y tamaño.
3.- Las propiedades de la materia varían según el agrupamiento de los átomos.
Aristóteles
En el siglo V a. C., Leucipo sostenía que había un sólo tipo de materia y pensaba que si dividíamos la materia en partes cada vez más pequeñas, obtendríamos un trozo que no se podría cortar más. Demócrito llamó a estos trozos átomos ("sin división").
La filosofía atomista de Leucipo y Demócrito podía resumirse en:
1.- Los átomos son eternos, indivisibles, homogéneos e invisibles.
2.- Los átomos se diferencian en su forma y tamaño.
3.- Las propiedades de la materia varían según el agrupamiento de los átomos.
Aristóteles
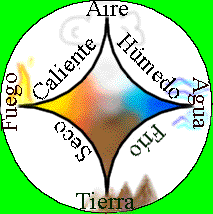
Aristóteles, posteriormente, postula que la materia estaba formada por esos 4 elementos pero niega la idea de átomo, hecho que se mantuvo hasta 200 años después en el pensamiento de la humanidad.
John Dalton

Durante el s.XVIII y principios del XIX algunos científicos habían investigado distintos aspectos de las reacciones químicas, obteniendo las llamadas leyes clásicas de la Química.
La imagen del átomo expuesta por Dalton en su teoría atómica, para explicar estas leyes, es la de minúsculas partículas esféricas, indivisibles e inmutables,
iguales entre sí en cada elemento químico.

J.J. Thomson

Demostró que dentro de los átomos hay unas partículas diminutas, con carga eléctrica negativa, a las que se llamó electrones.

De este descubrimiento dedujo que el átomo debía de ser una esfera de materia cargada positivamente, en cuyo interior estaban incrustados los electrones.
(Modelo atómico de Thomson.)

Demostró que dentro de los átomos hay unas partículas diminutas, con carga eléctrica negativa, a las que se llamó electrones.

De este descubrimiento dedujo que el átomo debía de ser una esfera de materia cargada positivamente, en cuyo interior estaban incrustados los electrones.
(Modelo atómico de Thomson.)

E. Rutherford

Demostró que los átomos no eran macizos, como se creía, sino que están vacíos en su mayor parte y en su centro hay un diminuto núcleo.

Dedujo que el átomo debía estar formado por una corteza con los electrones girando alrededor de un núcleo central cargado positivamente.
(Modelo atómico de Rutherford.)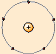

Demostró que los átomos no eran macizos, como se creía, sino que están vacíos en su mayor parte y en su centro hay un diminuto núcleo.

Dedujo que el átomo debía estar formado por una corteza con los electrones girando alrededor de un núcleo central cargado positivamente.
(Modelo atómico de Rutherford.)

Niels Bohr


Espectros atómicos discontinuos originados por la radiación emitida por los átomos excitados de los elementos en estado gaseoso.

Propuso un nuevo modelo atómico, según el cual los electrones giran alrededor del núcleo en unos niveles bien definidos.
(Modelo atómico de Bohr.)

Elaborado por:
Mauricio Garza Castillo
Marino Aguirre Saenz
Alejandro Jared Villarreal
Alexis Galicia Treviño